Cosa troverai in questo articolo:
- Una spiegazione dei 9 meccanismi biologici alla base delle patologie dell’invecchiamento
- Nell’invecchiamento, oltre ai danni al DNA, un ruolo fondamentale è giocato dall’epigeneticaLetteralmente “al di sopra della genetica”. Con questo termine s’intendono tutti i processi biochimici che, senza modificare la sequenza del DNA, incidono sulla espressione dei geni, sia “accendendoli” che “spegnendoli”.
- I meccanismi sono interconnessi ed è possibile modificarli con interventi mirati
Perché invecchiamo?
Per quanto complessa, oggi una risposta alla domanda “perché invecchiamo” può essere data. Anzi, se ne conoscono almeno nove. Un gruppo internazionale di ricercatori ha infatti individuato nove meccanismi chiave (hallmark) dell’invecchiamento nelle specie animali, esseri umani compresi. Come riportano gli scienziati nel loro studio pubblicato su Cell già nel 2013, questi meccanismi sono:
- .L’instabilità del genoma, cioè l’accumularsi progressivo di danni (mutazioni) nel DNA causati da agenti esterni, come alcune sostanze chimiche nocive, gli inquinanti, le radiazioni ionizzanti, il fumo e così via. Con il tempo le cellule perdono la capacità di ripararli e le mutazioni causano danni funzionali importanti alle cellule stesse, fino alla loro degenerazione tumorale.
- L’accorciamento dei telomeri, le parti finali dei cromosomi che, come dei cappucci, proteggono il DNA (rendendolo più stabile), e che si “consumano” ad ogni divisione cellulare. La scoperta è valsa il Premio Nobel per la Medicina e la Fisiologia nel 2009 alla biochimica australiana Elizabeth Blackburn e ai biologi Carol Greider e Jack Szostak.

- Le alterazioni epigenetiche: reazioni biochimiche che controllano “l’accensione” e lo “spegnimento” dei geni, incidendo anche sulla capacità di riparazione dei danni al DNA. Si tratta di cambiamenti reversibili, in cui l’ambiente e lo stile di vita hanno un ruolo fondamentale.
Le alterazioni epigenetiche sono cambiamenti reversibili in cui l’ambiente e lo stile di vita hanno un grande peso.
- La perdita di proteine sane (proteostasi). Tutte le cellule possiedono dei meccanismi di “controllo di qualità” delle proteine che vengono fabbricate e che contribuiscono alle funzioni cellulari. Se una proteina viene alterata e modificata in qualche modo fino a perdere la sua funzione originale, le cellule la scartano. Quando i meccanismi di scarto non funzionano correttamente, le proteine danneggiate si accumulano e creano danni che possono essere permanenti.
- Le alterazioni dei meccanismi che permettono la corretta percezione del fabbisogno di nutrienti, dovute a cambiamenti del metabolismo. L’esempio più conosciuto è la perdita di risposta all’insulinaOrmone prodotto dalle cellule delle isole di Langerhans del pancreas. Stimola l’ingresso del glucosio nelle cellule, sottraendolo al sangue e abbassando quindi la glicemia. Essa induce l'utilizzo del glucosio sia per produrre energia, che per la sintesi del glicogeno e dei grassi. (insulino-resistenza), l’anticamera del diabete. Per controllare la glicemia, le cellule del pancreas sono costrette a produrre sempre più insulina fino ad esaurirne le scorte. L’insulino-resistenza è strettamente collegata ad altri meccanismi dell’invecchiamento, primo fra tutti l’infiammazione cronica latente (inflammaging“Infiammazione cronica di basso grado” o inflammaging, e cioè uno stato di infiammazione organica di bassa intensità ma costante (associato all’aumento di alcune proteine, le citochine infiammatorie) che provoca danni all’organismo.).
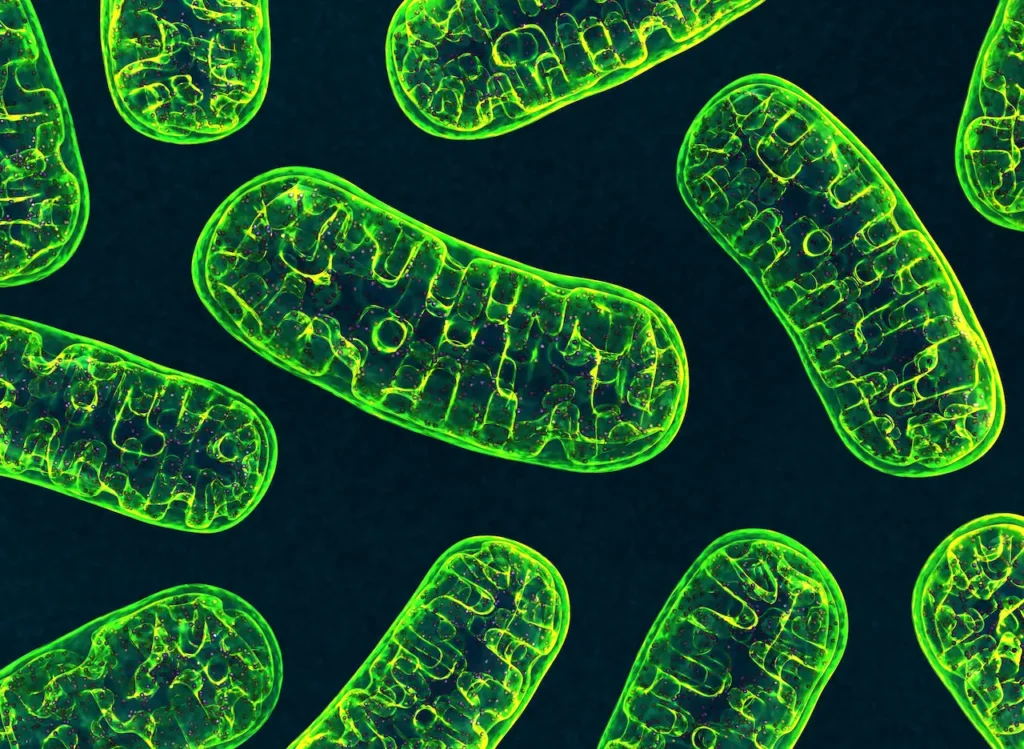
- Le disfunzioni dei mitocondri, gli organelli che rappresentano la centrale energetica della cellula. I mitocondri hanno un loro DNA (che si eredita solo per via materna) con un numero limitato di geni, che però svolgono funzioni molto importanti. Il DNA mitocondriale è costantemente soggetto a danni da stress ossidativo a causa dei radicali liberiUn radicale libero è una molecola o un atomo particolarmente reattivo che contiene almeno un elettrone spaiato nel suo orbitale più esterno. A causa di questa caratteristica chimica, i radicali liberi sono altamente instabili e cercano di tornare all'equilibrio rubando all'atomo vicino l'elettrone necessario per pareggiare la propria carica elettromagnetica. Questo meccanismo dà origine a nuove molecole instabili, innescando una reazione a catena che, se non viene arrestata in tempo, finisce col danneggiare le strutture cellulari ed i processi metabolici. prodotti come conseguenza delle reazioni che avvengono nei mitocondri stessi.
- La senescenza cellulare indipendente dai meccanismi visti finora, con il conseguente accumulo di “cellule zombie” che infiammano i tessuti. Sebbene non funzionino più, infatti, queste cellule non muoiono perché hanno perso la capacità di auto-eliminarsi alla fine del loro ciclo vitale, da cui il nome “zombie”. Rappresentano una piccola frazione di tutte le cellule che costituiscono un tessuto, ma provocano danni alle cellule circostanti, producendo fattori infiammatori (citochineLe citochine sono proteine di piccole dimensioni prodotte dal sistema immunitario, che si legano a specifici recettori presenti sulla membrana e comunicano alla cellula un'istruzione specifica come, ad esempio, lo stimolo a crescere, oppure a differenziarsi o ancora l'ordine di morire. Vengono prodotte da diversi tipi di cellule e, una volta liberate nell'organismo, inducono specifiche reazioni nelle cellule adiacenti (effetto paracrino), in altre molto lontane (effetto endocrino) oppure in quelle che le hanno create (effetto autocrino).) che a loro volta creano un microambiente infiammatorio che danneggia il tessuto stesso.
- La perdita della capacità rigenerativa dei tessuti, legata all’esaurimento delle cellule staminali. I meccanismi alla base dell’esaurimento delle cellule staminali sono molteplici, ma la risposta a questo problema non è così complicata come potrebbe sembrare.
- L’alterazione della comunicazione tra le cellule, con la produzione di molecole infiammatorie. È uno dei meccanismi più studiati dell’invecchiamento, anche chiamato inflammaging, ed è anche quello su cui è possibile intervenire efficacemente con interventi sullo stile di vita (dieta e esercizio fisico moderato regolare) e con integrazioni nutrizionali mirate.
L’epigenetica è facilmente influenzabile e la scienza ha già scoperto come farlo
Non solo DNA
Risulta evidente che l’invecchiamento è un fenomeno multidimensionale, che coinvolge anche il sistema immunitario e ormonale. L’accumulo di danni al DNA è stato storicamente considerato come la causa principale, e anche quella su cui è più difficile intervenire, ma la prima buona notizia è che le cellule posseggono già meccanismi capaci di prevenire questi danni ed eventualmente ripararli. Dei nove meccanismi citati, inoltre, quelli epigenetici sembrano giocare un ruolo centrale: tutti gli altri possono essere ricollegati al malfunzionamento dei sistemi di controllo epigenetici, e non a caso oggi si parla con sempre più convinzione di “invecchiamento epigenetico” o epigenetic drift, come proposto da David D. Sinclair, professore di Genetica all’Harvard Medical School e co-direttore del Paul F. Glenn Center for the Biology of Aging, nel libro Lifespan.
L’invecchiamento è un fenomeno multidimensionale in cui i meccanismi epigenetici hanno il peso maggiore
Una caratteristica interessante delle cause alla base dell’invecchiamento è la loro stretta interdipendenza: i differenti meccanismi si influenzano a vicenda. Questo vuol dire che se si migliora anche soltanto uno di questi, miglioreranno automaticamente anche tutti gli altri. E qui arriviamo alla seconda buona notizia: l’epigenetica è facilmente influenzabile dagli stili di vita e la ricerca ha identificato molecole di origine naturale, farmaci e interventi mirati capaci di rimettere in funzione i suoi meccanismi.
Se si migliora anche soltanto su uno dei 9 meccanismi, miglioreranno automaticamente tutti gli altri
Nel 2023, lo stesso gruppo di ricerca che aveva descritto i 9 hallmark dell’invecchiamento ha annunciato, sempre sulla rivista scientifica Cell, l’individuazione di tre ulteriori indicatori: l’infiammazione cronica di basso grado (inflammaging), la disregolazione di specifici meccanismi che regolano lo smaltimento dei rifiuti tossici all’interno delle cellule (disattivazione della macroautofagia) e l’alterazione del microbiota intestinale (disbiosi). Qui il link per approfondirli e scoprire quali connessioni hanno con i primi 9 hallmark.





